CELL|科研团队揭示肝纤维化与血管新生新机制
来源: 本网 作者: 本网 日期: 2019-08-30
我国是肝病大国,约有4亿肝病患者,肝病发病率和死亡率均高于世界平均水平。肝病患者绝大部分是慢性肝病,慢性肝病的特点是炎症和不断进展的纤维化(Fibrogenesis)。肝纤维化是一个动态过程,起因于多种病因引起的肝细胞损伤,包括毒素、酒精、肝炎病毒、非酒精性脂肪病变、自身免疫性肝炎等。肝脏受损时会产生生理性修复反应试图维持正常组织功能,然而该修复反应却往往导致肝纤维化,反而使细胞功能丢失、组织结构受损、乃至致死性器官功能衰竭,相当部分的肝癌患者也是由肝纤维化肝硬化演变而来。因此,针对肝纤维化发生发展机制及其治疗方法的研究将有可能为治疗大部分肝脏疾病带来希望。目前世界上尚无有效药物来治疗肝纤维化,突破肝纤维化治疗瓶颈将产生极大的社会效益和经济效益。
2019年8月29日,南方医科大学周伟杰教授带领其团队成员在Cell杂志上在线发表了题为LECT2, a Ligand for Tie1, Plays a Crucial Role in Liver Fibrogenesis的研究论文,揭示了LECT2-Tie1信号通路通过调控肝脏门脉血管新生和肝血窦毛细血管化进而调控肝纤维化进程的新机制,并提出了应区别对待门脉血管新生和肝血窦毛细血管化在肝纤维化进展中的不同作用的新观念。该项研究得到了广州再生医学与健康广东省实验室相关课题的资助。
Tie (tyrosine kinase with immunoglobulin-like and epidermal growth factor homology) 家族酪氨酸激酶受体主要由Tie1、Tie2组成,最初于1992年被报道。它们被认为在血管新生和稳态维持中发挥重要作用,也一直被认为是血管内皮细胞的标志物。其中Tie2的功能和机制研究的比较成熟,与多个配体结合调控血管新生和稳态维持,在发育和多种疾病中扮演重要角色。Tie1的功能也非常重要,其基因敲除小鼠会导致中晚期胚胎发育因严重的出血和微血管异常而致死,但它的配体一直未被找到,二十多年来一直作为孤儿受体(orphan receptor)存在,其下游调控机制也不清楚,Tie1在肝纤维化进程中的作用和机制此前未见报道。LECT2是一个分子量约16KD的分泌蛋白,最初作为炎症细胞诱导因子被报道,参与多种生理病理进程,其在肝纤维化进程中的作用和调控机制此前尚不明确。
在本文中,研究者发现肝纤维化肝硬化临床病人中的外周血LECT2蛋白上调,血清LECT2水平与肝纤维化肝硬化临床分级高度相关。这表明,血清LECT2水平有作为肝硬化生物标志物的潜力。目前市面上尚无灵敏有效的肝纤维化肝硬化血液诊断分子标志物,这个发现将有可能填补这一空白。
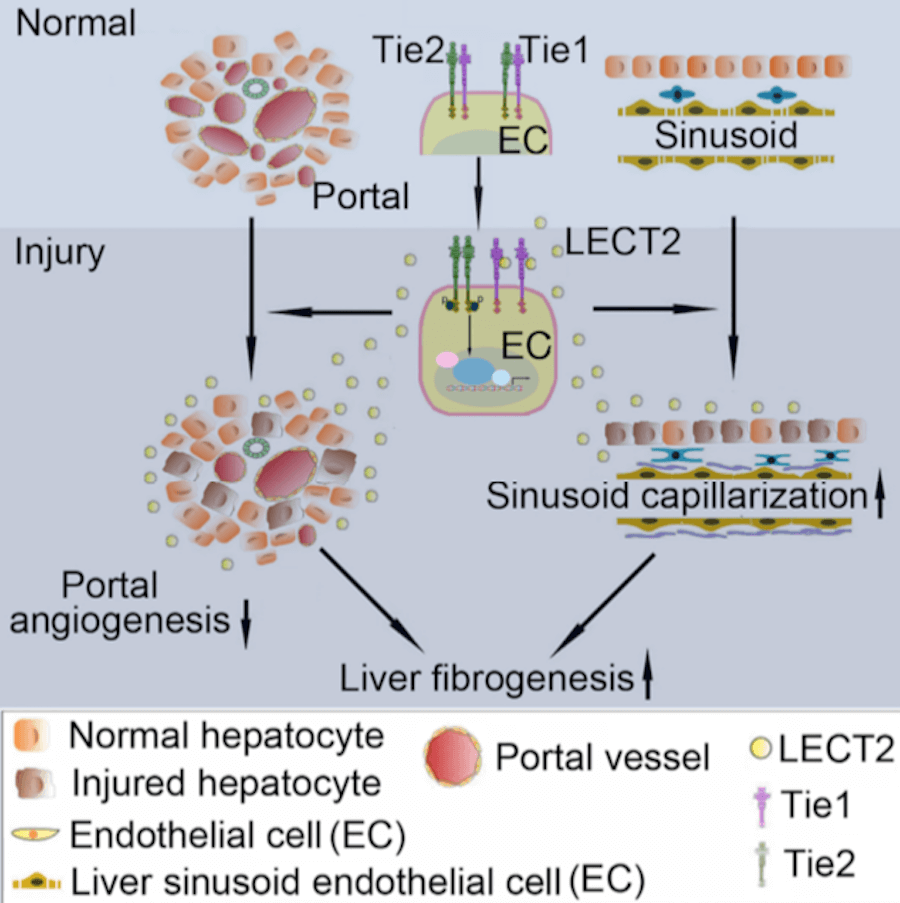
研究者通过多种小鼠肝纤维化模型发现,LECT2过表达小鼠肝纤维化加重,而LECT2基因敲除小鼠肝纤维化病情减轻,利用腺相关病毒敲低小鼠体内LECT2表达对肝纤维化有明显的治疗效果。更重要的是,研究者注意到肝纤维化进程中汇管区血管新生和肝血窦毛细血管化发生了不同的变化,这可能是肝纤维化发生发展的关键影响因素。研究者指出,肝血窦毛细血管化促肝纤维化,而门脉血管新生抑制肝纤维化,这可能是为什么血管抑制剂临床上治疗肝纤维化效果不好的重要原因。从干预血管的角度治疗肝纤维化,须同时考虑抑制肝血窦毛细血管化和促进门脉血管新生才有可能有较好的效果。从这个角度看,LECT2是一个比较好的干预靶点。
科研人员进一步发现,LECT2能够与血管内皮细胞Tie1受体直接结合并调控血管内皮细胞功能,为孤儿受体Tie1找到了功能配体。在下游信号机制研究中发现,LECT2-Tie1结合促进Tie1/Tie2异源二聚体解离,Tie2/Tie2同源二聚体增多,磷酸化增强,激活下游MAPK/PPAR/MMP/VE-cadherin信号通路,调控血管内皮细胞迁移和血管形成及肝纤维化进程。

LECT2-Tie1信号通路示意图
该研究为孤儿受体Tie1找到了功能配体并深入探讨了LECT2-Tie1信号通路在肝纤维化进程中的重要作用和机制。提出了应区别对待门脉血管新生和肝血窦毛细血管化在肝纤维化进展中的不同作用的新观念。该研究不仅为我们提供了新的肝纤维化肝硬化血液诊断分子标志物和肝纤维化肝硬化干预治疗靶标,还可以加深人们对血管系统调控的进一步理解,为其他组织器官血管系统相关疾病的研究提供有益借鉴。
该项研究由南方医科大学周伟杰教授指导完成,南方医科大学徐濛博士、徐洪海博士、林媛博士为本文的共同第一作者,南方医科大学周伟杰教授、丁彦青教授为共同通讯作者。山东大学武大雷教授及其博士生孙向楠、广东药科大学王丽京教授、温州医科大学方哲平教授、悉尼大学乔梁教授等合作者为本研究做出了重要贡献。
原文链接:https://doi.org/10.1016/j.cell.2019.07.021